Silikat nedir? Silikat türleri ve endüstriyel kullanım alanları hakkında eksiksiz rehber (6 başlık)

Silikat nedir?
- Silikat nedir? Basit bilimsel tanım
- Silikatların keşif tarihi
- Kimyasal yapı ve SiO₄ tetrahedronu
- Silikat türleri (7 ana grup)
- Önemli endüstriyel ve ticari silikatlar
- Silikatların çeşitli endüstrilerde kullanım alanları 1404
- Sodyum silikat (su camı) nedir?
- Silikat ile silis arasındaki fark
- Sağlık riskleri ve güvenlik önlemleri
- 2030’a kadar silikatların ve nanosilikatların geleceği
- Sıkça sorulan sorular
Silikat nedir? Basit ve anlaşılır bilimsel tanım
Silikatlar, Dünya kabuğundaki en büyük ve en önemli mineral grubudur; katı kabuğun %90’ından fazlasını ve toplam kütlenin yaklaşık %75’ini oluştururlar.
Basitçe söylemek gerekirse: Yapısında silikon (Si) ve oksijen (O) bulunan ve genellikle sodyum, potasyum, kalsiyum, magnezyum, alüminyum veya demir gibi metallerle birleşmiş her bileşik bir silikattır.
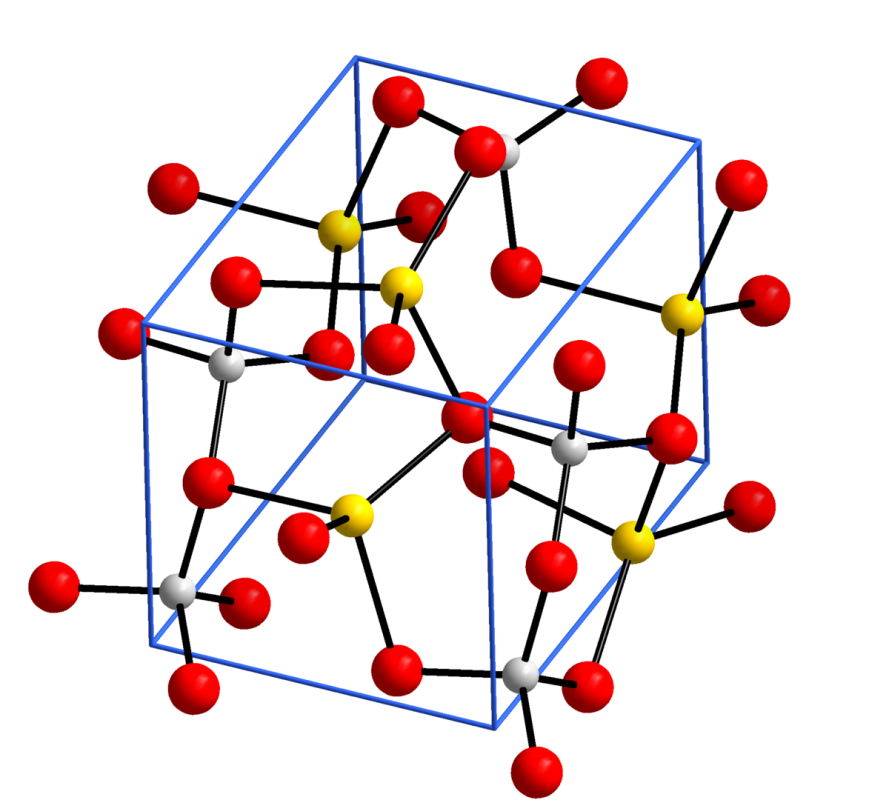
Tüm silikatların temel yapısal birimi, merkezde bir silikon atomu ve köşelerde dört oksijen atomu bulunan [SiO₄]⁴⁻ tetrahedronudur.

Bu tetrahedronlar çeşitli şekillerde birbirine bağlanabilir ve 7 ana silikat yapısı oluşturur. Aşağıda bunları detaylı olarak inceleyeceğiz.
Silikatların keşif ve araştırma tarihi
Silikatlara yönelik bilimsel keşif 18. yüzyılda başlamıştır:
- 1789 – Antoine Lavoisier, silisi yeni bir element olarak tanımladı
- 1811 – Jöns Jakob Berzelius, SiO₄ tetrahedron yapısını önerdi
- 1930 – William Lawrence Bragg ve ekibi, X-ışını kırınımı ile silikatların kesin yapısını doğruladı
- 1950–1970 – Union Carbide ve Mobil Oil tarafından sentetik zeolitlerin geliştirilmesi
- 1990’lar – Tabakalı ve mezoporlu nanosilikatların endüstriyel üretimi
- 2020 sonrası – Lityum piller, ilaç taşıma ve CO₂ yakalama teknolojilerinde nanosilikat uygulamaları
Silikatların kimyasal yapısı ve SiO₄ tetrahedronu
Silikatlar, [SiO₄]⁴⁻ tetrahedronlarının birbirlerine bağlanma biçimine göre sınıflandırılır. Bu bağlanma tipi, silikatların fiziksel özelliklerini (sertlik, erime noktası, çözünürlük, yoğunluk) doğrudan belirler.
SiO₄ birimlerinin bağlanma tipleri:
- Bağımsız (nesosilikatlar): Tetrahedronlar birbirine bağlı değildir.
- Çift tetrahedron (sorosilikatlar): İki tetrahedron bir oksijen paylaşır.
- Halkalı (siklosilikatlar): 3, 4 veya 6 tetrahedron halkaları.
- Zincir (inosilikatlar): Tek veya çift zincir yapıları.
- Tabaka (fillosilikatlar): İki boyutlu ince tabakalı yapı.
- İskelet (tekto-silikatlar): Üç boyutlu ağ yapısı.

Bu sınıflandırma aşağıdaki ana grupları oluşturur.
7 ana silikat türü
Aşağıda tüm silikat grupları dünya mineralojisinde kabul edilen şekliyle listelenmiştir:
- Nesosilikatlar (ada silikatları) – Olivin, zirkon, granat
- Sorosilikatlar – Epidot, vesuvianit
- Siklosilikatlar – Beril, tourmalin
- İnosilikatlar
- Tek zincir → Piroksen grubu
- Çift zincir → Amfibol grubu
- Fillosilikatlar – Mika, talk, kaolinit, bentonit
- Tektosilikatlar – Kuvars, feldispatlar, zeolitler
- Özel sentetik silikatlar – Mezoporlu MCM-41, SBA-15, nanosilikatlar
Endüstride kullanılan en önemli silikatlar
Aşağıda sanayi, kimya, seramik, metalurji ve inşaat sektörlerinde en çok kullanılan silikat bileşikleri listelenmiştir:
1. Sodyum silikat (Na₂SiO₃ – Su camı)
- Yapıştırıcı ve bağlayıcı
- Detarjan ve yüzey aktif madde üretimi
- Yangın geciktirici kaplamalar
- Su izolasyonu ve yapı kimyasalları
2. Potasyum silikat (K₂SiO₃)
- Yüksek sıcaklık dayanımlı kaplamalar
- Isıya dayanıklı yapıştırıcılar
- Yüksek kaliteli mineral boya bağlayıcısı
3. Kalsiyum silikat
- İzolasyon panelleri
- Çimento ve refrakter malzemeler
- Kimyasal emici ajanlar
4. Alüminosilikatlar
- Katalizör destek maddeleri
- Seramik ve cam üretimi
5. Zeolitler
- Petrol rafinerilerinde katalizör
- Su arıtma ve iyon değiştirme
- Koku ve nem emici
6. Nanosilikatlar
- Kompozit güçlendirme
- İlaç taşınım sistemleri
- Yüksek yüzey alanlı adsorbanlar
Silikatların endüstrilerde geniş kullanım alanları
Aşağıdaki tablo, silikatların farklı sektörlerdeki en önemli kullanım alanlarını özetler:
| Endüstri | Kullanım alanı |
|---|---|
| Kimya | Detarjan, adsorban, katalizör |
| İnşaat | Su yalıtımı, çimento, zemin kaplamaları |
| Petrol & Gaz | Zeolit katalizörleri |
| Seramik | Cam, porselen, sır bileşenleri |
| Elektronik | Yalıtkan tabakalar, mikro gözenekli dielektrikler |
| Çevre | Atık su arıtımı, ağır metal tutucu |
Sodyum silikat (su camı) nedir?
Sodyum silikat, en yaygın ticari silikat türüdür ve Na₂SiO₃ genel formülüyle bilinir. Su ile kolayca çözünebilen bir cam benzeri katıdır.
Özellikleri:
- Yüksek pH (alkalik)
- Güçlü bağlayıcı
- Yangın geciktirici
- Beton ve mineral yüzeylerle güçlü etkileşim
Kullanım alanları:
- Detarjan üretimi
- Inşaatta su yalıtımı
- Döküm sanayi
- Kağıt ve karton güçlendirme
- Metal temizleme kimyasalları
Silikat ile silis (SiO₂) arasındaki fark nedir?
Bu iki terim sıkça karıştırılır, ancak farklıdır:
| Özellik | Silikat | Silis (SiO₂) |
|---|---|---|
| Tanım | SiO₄ tetrahedronu ve metal iyonları içeren bileşikler | Saf silikon dioksit |
| Bileşim | Si + O + metal iyonları | Si + O |
| Çözünürlük | Birçok silikat çözünür | Silis çoğunlukla çözünmez |
| Kullanım | Detarjan, çimento, cam, katalizör | Kum, kuvars, cam |
Özetle: tüm silisler, tektosilikat grubuna giren bir tür silikattır.
Silikatların sağlık etkileri ve güvenlik önlemleri
Potansiyel sağlık riskleri:
- Toz formunda solunması akciğer tahrişine yol açabilir
- Yüksek pH değerine sahip çözeltiler cildi tahriş eder
- Uzun süreli maruziyet solunum rahatsızlıklarını artırabilir
Güvenlik önerileri:
- Maske (P2/P3) kullanımı
- Eldiven ve gözlük ile çalışma
- İyi havalandırılmış ortam
- Cilt teması hâlinde bol su ile yıkama
2030’a kadar silikatların ve nanosilikatların geleceği
Bilimsel yayınlar ve endüstri raporları, nanosilikatların 2030 yılına kadar aşağıdaki alanlarda kritik rol oynayacağını göstermektedir:
- Lityum iyon piller: Silikat bazlı nano-kaplamalar ile daha uzun ömür
- CO₂ yakalama: Zeolit ve modifiye silikat adsorbanlar
- İlaç taşıma: Kontrollü salım yapan mezoporlu silis
- Yapı malzemeleri: Düşük karbonlu çimentolar için reaktif nanosilikatlar
- Membran teknolojisi: Su arıtımında nano-SiO₂ güçlendirmeleri
Bu nedenle silikatlar, hem geleneksel sanayide hem de ileri teknolojilerde önemini artırmaya devam edecektir.
Sıkça sorulan sorular
Silikatlar çözünür müdür?
Birçok sodyum ve potasyum silikat çözünürdür. Ancak kuvars (SiO₂) gibi silisler çözünmezdir.
En yaygın silikat türü hangisidir?
Yer kabuğunda en yaygın silikat grubu tektosilikatlardır; özellikle feldispatlar ve kuvars.
Silikatlar tehlikeli midir?
Katı formda genelde güvenlidirler. Ancak ince tozların solunması veya yüksek pH’lı çözeltilere çıplak elle dokunmak risklidir.
Sodyum silikat nerede kullanılır?
Detarjan, inşaat kimyasalları, döküm, su yalıtımı ve kağıt endüstrisinde yaygın olarak kullanılır.
Silis ile silikat aynı şey midir?
Hayır. Silis, saf SiO₂’dir; silikat ise metal iyonları içeren daha geniş bir gruptur.
Silikata mı ihtiyacınız var?
Ücretsiz teknik danışmanlık — Numune gönderimi — Rekabetçi fiyatlar — Hızlı teslimat
- WhatsApp veya Telegram üzerinden mesaj gönderin
- Resmi web sitesi üzerinden sipariş verin